Вариант 29
Часть 1.
Ответом к заданиям 1–25 является последовательность цифр. Цифры в ответах на задания 7, 8, 10, 14, 15, 19, 20, 22, 24 могут повторяться.
Определите, атомы каких из указанных в ряду элементов в основном состоянии имеют на внешнем энергетическом уровне один неспаренный электрон. Запишите в поле ответа номера выбранных элементов.
1. H
2. Cu
3. Mg
4. P
5. S
Из указанных в ряду химических элементов выберите три элемента, которые образуют летучие водородные соединения. Расположите выбранные элементы в порядке увеличения валентности в их летучих водородных соединениях.
1) S
2) P
3) Ar
4) Si
5) Mg
Из числа указанных в ряду элементов выберите два элемента, которые в кислотных оксидах проявляют одинаковую степень окисления.
1) C
2) Mg
3) Sc
4) Pb
5) Si
Из предложенного перечня выберите два вещества, в которых присутствует ковалентная полярная химическая связь.
1) натрий
2) угарный газ
3) иодид натрия
4) хлорид фосфора(III)
5) кислород
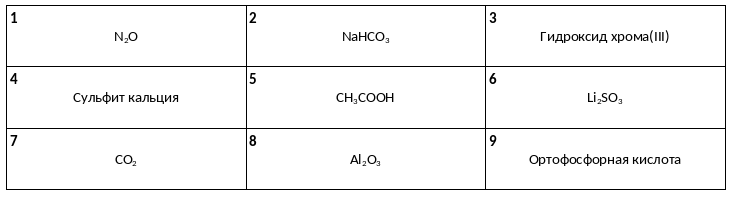
Среди предложенных веществ, расположенных в пронумерованных ячейках, выберите названия или формулы: А) кислотного оксида, Б) нерастворимой соли, В) одноосновной кислоты
К одной из двух пробирок с раствором иодида алюминия добавили раствор вещества X, а к другой – раствор вещество Y. В результате в первой пробирке наблюдалось выпадение, а затем растворение осадка, а во второй – выпадение желтого осадка. Из предложенного перечня выберите вещества X и Y, которые могут вступать в описанные реакции.
1) Na3PO4
2) KOH
3) Na2CO3
4) AgNO3
5) NH3
Установите соответствие между формулой вещества и реагентами, с каждым из которых это вещество может взаимодействовать: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ФОРМУЛА ВЕЩЕСТВА
А) Fe(OH)2
Б) FeCl3
В) CO2
Г) BaCl2
РЕАГЕНТЫ
1) НСl, C, CO2
2) H2O2, HCl, HNO3
3) Ca(OH)2, LiOH, KOH
4) H2, NaBr, Na2O2
5) AgNO3, Na2CO3, ZnSO4
Установите соответствие между формулой вещества и реагентами, с каждым из которых-это вещество может взаимодействовать: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ФОРМУЛА ВЕЩЕСТВА
А) H2S
Б) HCl
В) CO2
Г) Fe
РЕАГЕНТЫ
1) AgNO3, КМnO4, КОН
2) N2, I2, SO2
3) N2, O2, Fe
4) CuSO4, НСl, FeCl3
5) NaOH, C, Ca
Задана следующая схема превращений:
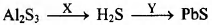
Определите, какие из указанных веществ являются веществами Хи Y.
1) НСl
2) NaOH
3) Н2
4) РbО
5) Pb(NO3)2
Установите соответствие между названием вещества и классом/группой, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
НАЗВАНИЕ ВЕЩЕСТВА
А) кумол
Б) крезол
В) изопрен
КЛАСС/ГРУППА
1) спирты
2) диены
3) арены
4) фенолы
Из предложенного перечня выберите два вещества, которые являются структурными изомерами метилацетата.
1) уксусная кислота
2) пропионовая кислота
3) этиленгликоль
4) этилформиат
5) стирол
Из предложенного перечня выберите все углеводороды, которые реагируют с аммиачным раствором оксида серебра(I).
1) этен
2) этин
3) бутен-2
4) бутин-2
5) пропин
Из предложенного перечня выберите два вещества, с которыми реагирует диметиламин.
1. HNO2
2. CH3Cl
3. CaCO3
4. CH3C(O)ONa
5. CH4
Установите соответствие между реагирующими веществами и органическим веществом, которое является продуктом реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) пропен и хлороводород
Б) ацетилен и водород (изб.)
В) пропин и вода
Г) циклопропан и бромоводород
ПРОДУКТ РЕАКЦИИ
1) этен
2) этан
3) 1-хлорпропан
4) 2-хлорпропан
5) ацетон
6) 1-бромпропан
Установите соответствие между реагирующими веществами и углеродсодержащим продуктом, который образуется при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) этилат натрия и бромметан
Б) этанол и бромоводород
В) уксусная кислота и натрий
Г) уксусная кислота и бром
ПРОДУКТ ВЗАИМОДЕЙСТВИЯ
1) бромуксусная кислота
2) ацетат натрия
3) этанол
4) метилэтиловый эфир
5) бромангидрид уксусной кислоты
6) бромэтан
Задана следующая схема превращений:
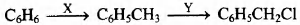
Определите, какие из указанных веществ являются веществами Х и Y.
1. CH4
2. CH3Cl
3. CH3NH2
4. Cl2
5. HCl
Реакция синтеза аммиака из азота и водорода является (выберите все верные ответы)
1. Некаталитической, необратимой
2. Каталитической, обратимой
3. Эндотермической, обратимой
4. Каталитической, необратимой
5. Экзотермической, соединения
Из предложенного перечня выберите все факторы, которые оказывают влияния на скорость реакции гидрирования дивинила в закрытом сосуде при поддержании постоянной температуры:
1. Повышение температуры окружающей среды
2. Изменение объема реакционного сосуда
3. Введение катализатора
4. Понижение концентрации водорода
5. Изменение формы реакционного сосуда
Установите соответствие между схемой реакции и свойством, которое проявляет элемент кислород в этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
СХЕМА РЕАКЦИИ
А) Na2O2 + CO2 → Na2CO3 + O2
Б) H2O + F2 → HF + O2
В) Fe(OH)2 + H2O2 → Fe(OH)3
СВОЙСТВО КИСЛОРОДА
1) только окислитель
2) только восстановитель
3) и окислитель, и восстановитель
4) не проявляет окислительно-восстановительных свойств
Установите соответствие между формулой соли и продуктами электролиза водного раствора этой соли, которые выделились на инертных электродах: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ФОРМУЛА СОЛИ
А) NaNO3
Б) AgF
В) AlCl3
Г) Na2SO4
ПРОДУКТЫ ЭЛЕКТРОЛИЗА
1) натрий,кислород
2) серебро, фтор
3) алюминий, хлор
4) водород, кислород
5) серебро, кислород
6) водород, хлор

Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л). Запишите номера веществ в порядке возрастания значения pH их водных растворов.
1) NH4NO3
2) CH3COOK
3) BaCl2
4) RbOH
Установите соответствие между уравнением химической реакции и направлением смещения химического равновесия при увеличении давления в системе: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
УРАВНЕНИЕ РЕАКЦИИ
А) SO2Cl2(г) ⇆ SO2(г) + Сl2(г)
Б) 2SO2(г) + О2(г) \leftrightarrows 2SO3(г)
В) 2Н2(г)+ 02(г) \leftrightarrows 2Н2O(г)
Г) S(г) + Н2(г) \leftrightarrows H2S(г)
НАПРАВЛЕНИЕ СМЕЩЕНИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ
1) в сторону продуктов реакции
2) в сторону исходных веществ
3) практически не смещается
В реактор постоянного объёма поместили N2H4 и водород. При этом исходная концентрация N2H4 составляла 0,55 моль/л. В результате протекания обратимой реакции N2H4 (г.) + H2 (г.) ⇋ 2NH3 (г.) В реакционной системе установилось химическое равновесие, при котором концентрации водорода и аммиака составили 0,32 моль/л и 0,18 моль/л соответственно. Определите исходную концентрацию водорода (X) и равновесную концентрацию N2H4 (Y).
Выберите из списка номера правильных ответов.
1) 0,09 моль/л
2) 0,37 моль/л
3) 0,41 моль/л
4) 0,46 моль/л
5) 0,50 моль/л
6) 0,55 моль/л
Установите соответствие между формулами веществ и реагентом, с помощью которого их можно различить: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ВЕЩЕСТВА
А) метил этил кетон и пропаналь
Б) пропанол-2 и глицерин
В) метиламин и триметиламин
Г) толуол и циклогексен
РЕАГЕНТ
1) Cu(OH)2
2) H2O
3) HNO2
4) Br2
5) NH3
В качестве удобрений используют нитраты:
1) аммония
2) бария
3) меди (II)
4) ртути (II)
5) калия
Какую массу воды нужно добавить к 30 г 20%-ного раствора гидроксида натрия, чтобы раствор стал 15%-ным?
Ответ:______________________г.
(Запишите число с точностью до целых.)
Какой объем кислорода необходим для окисления 20,2 л (н.у.) водорода?
Ответ:______________________л.
(Запишите число с точностью до десятых.)
Определите массу алюминия (г), который может быть получен из 6 кг технического оксида алюминия с содержанием основного вещества 93%. (Запишите число с точностью до целых.)
Часть 2.
Для записи ответов на задания 29–34 используйте БЛАНК ОТВЕТОВ. Запишите сначала номер задания (29, 30 и т. д.), затем подробное решение. Ответы записывайте чётко и разборчиво.
Для выполнения заданий 29 и 30 используйте следующий перечень веществ:
Сульфат натрия, гидрокарбонат бария, оксид меди(I), дихромат натрия, гидроксид натрия, серная кислота. Допустимо использование водных растворов веществ.
Из предложенного перечня веществ выберите вещества, между которыми может протекать окислительно-восстановительная реакция. В ходе реакции выделяется газ. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель.
Элементы ответа:
1) Написано уравнение реакции
Cu2O + 3H2SO4 = 2CuSO4 + SO2 + 3H2O
2) Указан электронный баланс
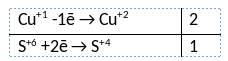
3) Указано, что сера в степени окисления +6 (серная кислота) является окислителем, а медь в степени окисления +1 (оксид меди(I)) является восстановителем.
Из предложенного перечня веществ выберите два вещества одного класса, которые вступают между собой в реакцию ионного обмена. В ходе реакции образуется осадок и не выделяется газ. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.
Элементы ответа:
1) Написано молекулярное уравнение:
Ba(HCO3)2 + Na2SO4 = BaSO4 + 2NaHCO3
2) Написано полное ионное уравнение:
Ba2+ + 2HCO3- + 2Na+ + SO42- = BaSO4 + 2Na+ + 2HCO3-
3) Написано сокращённое ионное уравнение:
Ba2+ + SO42- = BaSO4
Нитрат натрия сплавили с оксидом хрома (III) в присутствии карбоната натрия. Выделившийся при этом газ прореагировал с избытком гидроксида кальция с выпадением осадка белого цвета. Осадок растворили в избытке раствора бромоводородной кислоты и в полученный раствор добавили нитрат серебра до прекращения выделения осадка. Напишите уравнения описанных реакций.
1) 3NaNO3 + Cr2O3 + 2Na2CO3 = 2Na2CrO4 + 3NaNO2 + 2СO2
2) СO2 + Са(ОН)2 = СаСO3↓ + Н2O
3) СаСО3 + 2НВг = ВаВг2 + СO2↑ + Н2O
4) CaBr2 + 2AgNO3 = 2AgBr↓ + Ba(NO3)2
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
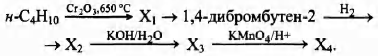
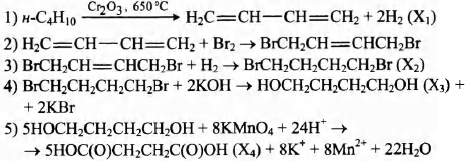
Для полного сгорания 12,0 г предельного одноатомного спирта потребовалось 20,16 л кислорода (н.у.).
1) произведите вычисления, необходимые для установления молекулярной формулы органического вещества;
2) запишите молекулярную формулу исходного органического вещества;
3) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле, если известно, что спирт является вторичным;
4) напишите уравнение его взаимодействия с бромоводородом.
2) С3Н8O;
3) С3Н7ОН;
4) СН3СН(ОН)СН3 + НВг → СН3СНВгСН3 + Н2O.
Смесь бромида калия и иодида калия растворили в воде. Полученный раствор разлили по трем колбам. К 250 г раствора в первой колбе добавили 430 г 40%-ного раствора нитрата серебра. После завершения реакции массовая доля нитрата серебра в образовавшемся растворе составила 8,44%. К 300 г раствора во второй колбе добавили избыток раствора нитрата меди (II), в результате чего в осадок выпало 28,65 г соли. Вычислите массовую долю каждой из солей в третьей колбе. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычислении (указывайте единицы измерения искомых физических величин).
Элементы ответа:
Записаны уравнения реакции:
(1) KBr + AgNO3 = AgBr + KNO3
(2) KI + AgNO3 = AgI + KNO3
(3) 2Cu(NO3)2 + 4KI = 2CuI + I2 + 4KNO3
Рассчитаны количество вещества реагентов и масса продуктов реакций:
В растворе во второй колбе было
n(KI) = 2n(CuI) = 2 • 28,65 / 191 = 0,3 моль
m(KI) = 0,3 • 166 = 49,8 г
ω(KI) = 49,9 / 300 = 0,166, или 16,6%
m(AgNO3) = 430 • 0,4 = 172 г
В растворе и первой колбе было
n(KI) = 0,3 • 250 / 300 = 0,25 моль
Пусть в растворе в первой колбе было
n(KBr) = x моль, тогда
m(AgNO3 прореаг) = 170 • (x + 0,25) г
m (образ. р-ра) = 250 + 430 − 188 • x − 235 • 0,25 = 621,25 − 188x г
(172 − 170x − 42,5) / (621,25 − 188x) = 0,0844
x = 0,5 моль
m(KBr) = 0,5 • 119 = 59,5 г
ω(KBr) = 59,5 / 250 = 0,238, или 23,8%
ω(KI) = 16,6%; ω(KBr) = 23,8%
| № | Ваш ответ | Ответ и решение | Первичный балл |
|---|---|---|---|
|
Здесь появится результат первой части. Нажмите на кнопку «Завершить работу», чтобы увидеть правильные ответы и посмотреть решения. |
|||