Задание № 31923
В реактор постоянного объёма поместили некоторое количество серы и водяного пара. При этом исходная концентрация водяного пара составляла 0,8 моль/л. В результате протекания обратимой реакции 3S (ж.) + 2H2O (г.) ⇋ 2H2S (г.) + SO2 (г.) в реакционной системе установилось химическое равновесие, при котором концентрация сероводорода составила 0,6 моль/л. Определите равновесные концентрации H2O (X) и SO2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л
2) 0,2 моль/л
3) 0,3 моль/л
4) 0,4 моль/л
5) 0,5 моль/л
6) 0,6 моль/л
[topic]
Для решения задачи необходимо составить таблицу, перенести в неё данные из условия и заполнить пропуски, пользуясь следующими правилами:
1) исходные концентрации продуктов всегда равны 0.
2) ΔС (изменение концентрации) находится как разность между равновесной концентрацией Сравн и исходной концентрацией Сисх (ΔC = Cравн – Cисх).
3) изменение концентрации разных участников реакции пропорционально коэффициентам в реакции и имеет противоположный знак у продуктов и реагентов.
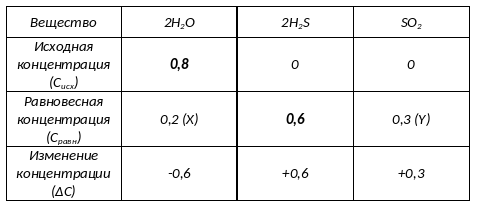
Жирным шрифтом выделены данные, известные из условия.
Ответ: 23Нашли ошибку в задании? Выделите фрагмент и нажмите Ctrl + Enter.