Задание № 19049
При сгорании 17,5 г органического вещества получили 28 л (н.у.) углекислого газа и 22,5 мл воды. Плотность паров этого вещества (н.у.) составляет 3,125 г/л. Известно также, что это вещество было получено в результате дегидратации третичного спирта.
На основании данных условия задачи:
1) произведите вычисления, необходимые для установления молекулярной формулы органического вещества;
2) запишите молекулярную формулу органического вещества;
3) составьте структурную формулу исходного вещества, которая однозначно отражает порядок связи атомов в его молекуле;
4) напишите уравнение реакции получения данного вещества дегидратацией соответствующего третичного спирта.
Общая формула вещества - СхНуOz
1) Найдены количество вещества углекислого газа, воды и органического вещества:
n(СO2) = 28 / 22,4 = 1,25 моль
n(Н2O) = 22,5 / 18 = 1,25 моль
M(СхНуОz) = 3,125 • 22,4 = 70 г/моль
n(CxHyOz) = 17,5 / 70 = 0,25 моль
2) Определена молекулярная формула вещества:
n(С) = n(СO2) = 1,25 моль
n(Н) = 2n(Н2O) = 2,5 моль
х = n(C) / n(CxHyOz) = 1 * 25 / 0,25 = 5
у = n(Н) / n(СхНуОz) = 2,5 / 0,25 = 10 5 • 12 + 10 + z • 16 = 70
z = 0
Молекулярная формула вещества - С5Н10
3) Составлена структурная формула вещества:
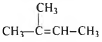
4) Составлено уравнение реакции получения вещества из третичного спирта:
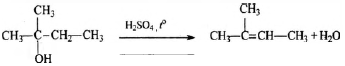
Нашли ошибку в задании? Выделите фрагмент и нажмите Ctrl + Enter.