Вариант 11
Часть 1.
Ответом к заданиям 1–26 является последовательность цифр. Цифры в ответах на задания 5, 10–12, 18, 19, 22–26 могут повторяться.
Два неспаренных электрона на внешнем уровне в основном состоянии имеют атомы:
1. Mg
2. C
3. O
4. Fe
5. Cl
1) Na 2) N 3) Si 4) Р 5) С
Из указанных в ряду химических элементов выберите три элемента, которые в Периодической системе химических элементов Д.И. Менделеева находятся в одном периоде. Расположите выбранные элементы в порядке возрастания окислительной способности простых веществ, образованных этими элементами. Запишите в поле ответа номера выбранных элементов в нужной последовательности.
1) Na 2) N 3) Si 4) Р 5) С
Из числа указанных в ряду элементов выберите два элемента, которые проявляют низшую степень окисления равную -3. Запишите в поле ответа номера выбранных элементов.
Из предложенного перечня выберите два соединения, в которых присутствует ковалентная полярная химическая связь.
1. СаСl2
2. НСl
3. ВаО
4. КСIO4
5. Сl2
Установите соответствие между формулой вещества и классом/группой, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ФОРМУЛА ВЕЩЕСТВА
А) Н2СO3
Б) СO2
В) N2O
КЛАСС/ГРУППА
1) кислота
2) оксид кислотный
3) оксид несолеобразующий
4) cоль кислая
Из предложенного перечня веществ выберите два вещества, с каждым из которых реагирует хлор.
1. сера
2. серная кислота
3. сульфат натрия
4. бромид натрия
5. фторид калия
Из предложенного перечня выберите два оксида, которые реагируют с водой, но не реагируют с гидроксидом натрия.
1. P2O5
2. SO3
3. CaO
4. FeO
5. Li2O
В пробирку с раствором соли X добавили несколько капель вещества Y. В результате реакции наблюдали выделение белого осадка. Из предложенного перечня выберите два вещества, которые могут вступать в описанную реакцию.
1. КОН
2. НСl
3. CuSO4
4. KNO3
5. Ba(NO3)2
Задана следующая схема превращений веществ:
LiX→LiOHY→LiCl
Определите, какие из указанных веществ являются веществами X и Y.
1. KCl(p-p)
2. Cu(OH)2
3. CuCl2 (р-р)
4. AgCI
5. Н2O
Установите соответствие между названием элемента и характерными степенями окисления, которые он может проявлять. К каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
НАЗВАНИЕ ЭЛЕМЕНТА
А) кислород
Б) бром
В) кремний
Г) железо
ХАРАКТЕРНЫЕ СТЕПЕНИ ОКИСЛЕНИЯ
1) -4, 0, +2, +4
2) 0, +2, +3, +6
3) -2, -1, 0, +2
4) 0, +2, +4, +6, +7
5) -1, 0, +1, +5, +7
Установите соответствие между формулой вещества и реагентами, с каждым из которых это вещество может взаимодействовать. К каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ФОРМУЛА ВЕЩЕСТВА
А) Zn(OH)2
Б) H2SO4 (разб.)
В) H2S
Г) Са
РЕАГЕНТЫ
1) LiOH, НNО3, НСl
2) NaOH, К2O, CuSO4.
3) H2O, S, HNO3
4) Zn, ВаСl2, NaHS
5) NaNO3, CuO, SiO2
Установите соответствие между названием вещества и классом/группой, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
НАЗВАНИЕ ВЕЩЕСТВА
А) пропен
Б) изопрен
В) ацетилен
КЛАСС/ГРУППА
1) арены
2) алкены
3) алкины
4) алкадиены
Из предложенного перечня выберите два вещества, которые являются структурными изомерами пропановой кислоты.
1. этиловый эфир муравьиной кислоты
2. пропанол-1
3. метилацетат
4. пропаналь
5. метилэтиловый эфир
Из предложенного перечня выберите два вещества, обесцвечивающие бромную воду.
1. бутадиен-1,3
2. бензол
3. гексан
4. стирол
5. пропан
Из предложенного перечня выберите два вещества, с которыми реагирует пропанол-2.
1. Cu
2. H2
3. HCl
4. CuO
5. Cu(OH)2
Из предложенного перечня выберите два вещества, с которыми реагирует анилин.
1. пропан
2. метан
3. бром
4. гидроксид натрия
5. соляная кислота
Задана следующая схема превращений веществ:
CH3CHCl2X→CH≡CHY→CH3CHO
Определите, какие из указанных веществ являются веществами X и Y.
1. H2O (Hg2+)
2. Zn
3. Cu(OH)2
4. NaOH (H2O)
5. NaOH (спирт)
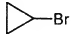
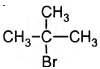
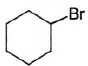
Установите соответствие между названием вещества и продуктом, который преимущественно образуется при взаимодействии этого вещества с бромом: к каждой позиции, обо знаменной буквой, подберите соответствующую позицию, обозначенную цифрой.
НАЗВАНИЕ ВЕЩЕСТВА
А) этан
Б) изобутан
В) циклопропан
Г) циклогексан
ПРОДУКТ БРОМИРОВАНИЯ
1) 
2) 
3) Вr-СН2-СН2-СН2-Вr
4) 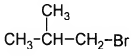
5) СН3-СН2-Вr
6) 
Установите соответствие между схемой реакции и веществом X, которое является одним из реагентов в ней: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
СХЕМА РЕАКЦИИ
А) фенол + X → фенолят калия
Б) муравьиная кислота + X → этилформиат
В) метаналь + X → углекислый газ
Г) этанол + X → этилат калия
ВЕЩЕСТВО X
1) СН3ОН
2) СuО
3) КМnО4(H+)
4) СН3СН2ОН
5) КНСО3
6) K
Из предложенного перечня выберите два типа реакций, к которым можно отнести взаимодействие азота с водородом.
1. каталитическая
2. гомогенная
3. необратимая
4. замещения
5. реакция нейтрализации
Из предложенного перечня выберите два внешних воздействия, которые приводят к уменьшению скорости реакции цинка с хлороводородной кислотой.
1. понижение температуры
2. уменьшение концентрации хлороводородной кислоты.
3. использование катализатора
4. уменьшение концентрации водорода
5. уменьшение давления в системе
Установите соответствие между формулой соли и продуктами электролита её водного раствора, которые выделились на инертных электродах: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ФОРМУЛА СОЛИ
А) CuSO4
Б) KNO3
В) CuBr2
Г) LiCl
ПРОДУКТЫ ЭЛЕКТРОЛИЗА
1) водород и кислород
2) металл и кислород
3) водород и галоген
4) металл и галоген
5) металл и водород
Установите соответствие между названием соли и её отношением к гидролизу: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ФОРМУЛА СОЛИ
А) СН3СООК
Б) Na2SO3
В) NH4CI
Г) NaCl
ОТНОШЕНИЕ К ГИДРОЛИЗУ
1) гидролиз по катиону
2) гидролиз по аниону
3) гидролиз по катиону и аниону
4) гидролизу не подвергается
Установите соответствие между уравнением химической реакции и направлением смещения химического равновесия при увеличении давления в системе: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
УРАВНЕНИЕ РЕАКЦИИ
А) N2(г) + 3H2(г) ⇄ 2NH3(г) + Q
Б) N2O4(г) \rightleftarrows 2NO2(г) - Q
В) CO2(г) + H2(г) \rightleftarrows CO(г) + H2O(г) - Q
Г) 4HCl(г) + O2 \rightleftarrows 2H2O(г) + 2Cl2(г) + Q
НАПРАВЛЕНИЕ СМЕЩЕНИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ
1) смещается в сторону продуктов реакции
2) смещается в сторону исходных веществ
3) смещение равновесия не происходит
Установите соответствие между формулами веществ и реагентом, с помощью которого можно различить их водные растворы: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
НАЗВАНИЯ ВЕЩЕСТВ
А) этанол-1 и фенол (р-р)
Б) крахмал и сахароза(кр.)
В) пропанол-2 и глицерин
Г) толуол и бензол
РЕАКТИВ
1) NaMnO4 (р-р)
2) ZnO
3) Br2 (водн.)
4) Сu(ОН)2
5) I2(р-р)
Установите соответствие между процессом и аппаратом, в котором он протекает: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ПРОЦЕСС
А) получение сернистого газа из пирита
Б) окисление оксида серы(IV)
В) очистка сернистого газа от оставшихся мелких частиц пыли
Г) получение серной кислоты из оксида серы(VI)
АППАРАТ
1) поглотительная башня
2) контактный аппарат
3) аппарат «Циклон»
4) электрофильтр
5) печь для обжига в «кипящем слое»
Смешали 400 г раствора с массовой долей азотной кислоты 25% и 200 г раствора с массовой долей этой кислоты 20%. Чему равна массовая доля кислоты в полученном растворе?
Ответ: ____________% (Запишите число с точностью до десятых.)
В результате реакции, термохимическое уравнение которой
С6Н12O6(тв.) + 6O2(г) = 6СО2(г) + 6Н2О(г) + 2800 кДж,
выделилось 560 кДж теплоты. Чему равно количество вещества кислорода, вступившего в реакцию?
Ответ: ________________ моль (Запишите число с точностью до десятых.)
Определите объём (н.у.) газа, выделившегося при растворении 44 г сульфида железа(II) в избытке соляной кислоты. (Запишите число с точностью до десятых.)
Ответ: ______________л
Часть 2.
Запишите сначала номер задания (30, 31 и т. д.), затем подробное решение. Ответы записывайте чётко и разборчиво.
Используя метод электронного баланса, составьте уравнение реакции:
KIO3 + KI + ... → I2 + K2SO4 + ...
Определите окислитель и восстановитель.
Элемента ответа:
1) Составлена электронный баланс:
1\;\vert\;2I^{+5}+10\overline e\rightarrow I_2^0
5\;\vert\;2I^{-1}+2\overline e\rightarrow I_2^0
2) Указано, что иодид калия (за счет иода в степени окисления - 1) является восстановителем, а иодид каклия (за счет иода в степени окисления +5) - окислителем.
3) Определены недостающие вещества, и расставлены коэффициенты в уравнении реакции:
КIO3 + 5KI + 3H2SO4 = 3I2+ 3K2SO4 + ЗН2O
Цинк полностью растворили в концентрированном растворе гидроксида калия. Образовавшийся прозрачный раствор выпарили, а затем прокалили. Твёрдый остаток растворили в необходимом количестве соляной кислоты. К образовавшемуся прозрачному раствору добавили сульфид аммония и наблюдали образование белого осадка. Напишите уравнения четырёх описанных реакций.
1)\;Zn\;+\;2KOH+2H_2O\;=\;K_2\lbrack Zn(OH)_4\rbrack+H_2\uparrow
2)\;K_2\lbrack Zn(OH)_4\rbrack\xrightarrow{t^\circ}K_2ZnO_2+2H_2O
2)\;K_2ZnO_2+4HCl=Zn_2+2KCl+2H_2O
4)\;ZnCI_2\;+\;(NH_4)_2S\;=\;ZnS\downarrow+\;2NH4CI
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
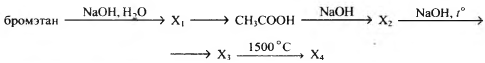
При написании уравнений реакций используйте структурные формулы органических веществ.
1)\;CH_3-CH_2-Br\;+\;NaOH\;\rightarrow CH_3-CH_2-OH\;+\;NaBr
2)\;5CH_3CH_2OH\;+\;4KMnO_{}4\;+\;6H_2SO_4\xrightarrow{t^\circ}
\rightarrow5CH_3COOH\;+\;4MnSO_4\;+\;2K_2SO_4\;+\;11H_2O
3)\;CH_3COOH\;+\;NaOH\rightarrow CH_3COONa\;+\;H_2O
4)\;CH_3COONa\;+\;NaOH\;\xrightarrow{t^\circ}\;CH_4\;+\;Na_2CO_3
5)\;2CH_4\;\xrightarrow{t^\circ}\;CH\equiv CH\;+\;3H_2
При сливании 160 г 10%-ного раствора нитрата бария и 50 г 11%-ного раствора хромата калия выпал осадок. Рассчитайте массовую долю нитрата бария в образовавшемся растворе. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения физических величин).
Возможно образование С и H2
1) Записано уравнение реакции:
Ba(NO3)2 + К2СrO4 = ВаСrO4 + 2KNO3
2) Рассчитаны количество вещества реагентов, и определено вещество, взятое в избытке:
n(Ba(NO3)2) = 160 • 0,1 / 261 = 0,061 моль
n(К2СrO4) = 50 • 0,11 / 194 = 0,028 моль
Ba(NO3)2 - в избытке
3) Рассчитаны масса выпавшего осадка и масса образовавшегося при этом раствора:
n(ВаСrO4) = n(К2СrO4) = 0,028 моль
n(ВаСrO4) = 0,028 моль • 253 г/моль = 7,08 г m(раствора) = 160 + 50 - 7,08 = 202,92 г
4) Рассчитаны масса нитрата бария и его массовая доля в растворе:
n(Ba(NO3)2)изб. = 0,061 - 0,028 = 0,033 моль
m(Ba(NO3)2) = 0,033 • 261 = 8,61 г
w(Ba(NO3)2) = m(Ba(NO3)2) / m(p-pa) = 8,61 / 202,92 = 0,042 или 4,2%
Некоторое органическое соединение содержит 40,0% углерода и 53,3% кислорода по массе. Известно, что это соединение реагирует с оксидом меди(II).
На основании данных условия задачи:
1) произведите вычисления, необходимые для установления молекулярной формулы органического вещества;
2) запишите молекулярную формулу органического вещества;
3) составьте структурную формулу исходного вещества, которая однозначно отражает порядок связи атомов в его молекуле;
4) напишите уравнение реакции этого вещества с оксидом меди(II).
Общая формула вещества - CxHyOz
1) Найдено соотношение атомов углерода, водорода и кислорода в соединении:
w(H) = 100 - 40,0 - 53,3 = 6,7%
х : у : z = 40/12 : 6,7/1 : 53,3/16 = 3,33 : 6,7 : 3,33 = 1:2:1
2) Определена молекулярная формула вещества.
Простейшая формула вещества - СН2O. Учитывая то, что вещество реагирует с оксидом меди(II), молекулярная формула вещества - С2Н4O2
3) Составлена структурная формула вещества:
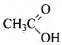
4) Составлено уравнение реакции с оксидом меди(II):
2СН3СООН + СuО → (СН3СОО) 2Сu + Н2O
| № | Ваш ответ | Ответ и решение | Первичный балл |
|---|---|---|---|
|
Здесь появится результат первой части. Нажмите на кнопку «Завершить работу», чтобы увидеть правильные ответы и посмотреть решения. |
|||